欢迎各位来到“circRNA研究报道汇总”栏目,本期从pubmed中检索收集最新发布(20230213-0219)的circRNA文献共计28篇,下面我们一起来看看,circRNA研究最近有哪些新进展。
检索式:(circRNA[Title/Abstract]) OR circular RNA[Title/Abstract]
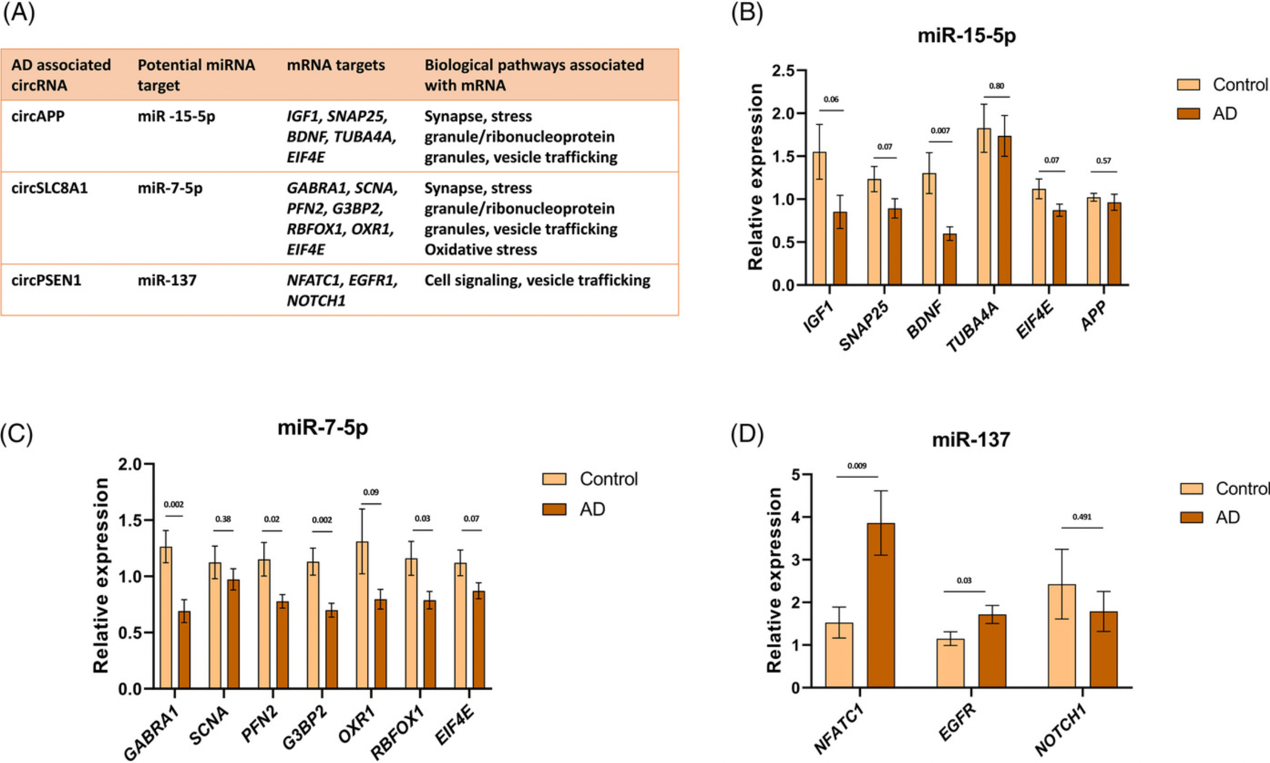
阿尔茨海默氏症(AD)是一种复杂的神经退行性疾病,是痴呆症最常见的原因。最近的基因组研究发现了数千个表达良好、稳定的circRNAs,这些circRNA在神经元组织中更丰富,并通常来自神经元和突触功能特异性的基因。circRNAs的发现为AD和相关痴呆症(ADRD)的神经变性机制研究提供了新思路。
在这项研究中,作者进行了全环状转录组分析,并检查了与人类海马体和皮层大脑区域的AD以及临床和神经病理AD严重程度相关的circRNA表达模式。作者还验证了之前对AD皮层circRNA的研究,并展示了AD海马体中新的表达模式。研究显示AD相关circRNA预测mRNA靶点的表达方式发生了变化。作者还表明,circRNA的表达因痴呆亚型而异,展示了人类神经元前体细胞(NPC)中强劲的circRNA表达,作者通过使用NPC研究定量聚合酶链式反应(qPCR)验证的circRNA,表明暴露于寡聚tau会引起类似于AD大脑观察到的circRNA的下调。
环状RNA(circRNA)是一组非编码、共价不间断的环转录物,其中大部分仍有待功能表征。在该项研究中,作者确定circPDIA4是胃癌中的致癌circRNA。临床上,circPDIA4在恶性组织中显著上调,并与癌症患者的低生存率相关。
circPDIA4的生物发生由RNA结合蛋白Quaking介导,Quaking结合PDIA4前mRNA的内含子2和4,以促进外显子3和4的反折叠。circPDIA4的高表达促进了体内各种小鼠异种移植模型的远处转移,并加速了体外癌症细胞的侵袭。circPDIA4通过细胞质和细胞核中不同的致癌机制发挥作用。细胞质circPDIA4与ERK1/2结合,并通过阻止DUSP6介导的ERK1/2去磷酸化来维持MAPK通路的过度激活。值得注意的是,circPDIA4缺失增强了癌症细胞对ERK抑制剂的敏感性。在细胞核中,circPDIA4作为诱饵与DHX9相互作用,并抑制其对circRNA生物发生的抑制功能,以促进多种致癌circRNA的表达,从而促进癌症的进展。这些发现揭示了circPDIA4通过调节致癌circRNA生物发生和增加MAPK活性的双重肿瘤促进机制。circPDIA4作为癌症潜在的预后生物标志物和治疗靶点应进一步研究。
CRC(结直肠癌)仍然是中国发病率和死亡率最高的癌症之一。新生血管化和血管生成是生理系统中输送营养物质的稳态过程。目前,抗血管生成剂被用于转移性CRC的靶向治疗,但仍有一些转移性CRC患者没有从中受益。因此,对肿瘤血管生成的进一步理解仍需探索。
外泌体是一类直径约为30至150 nm的囊泡,最近,越来越多的研究报告外泌体可以成为改变肿瘤微环境并导致肿瘤转移的细胞间通信的媒介。此外,来自癌症细胞或其他细胞(如M2巨噬细胞)的外显子中的非编码RNA在血管生成和肿瘤转移中起着关键作用。circRNA是一类结构稳定的非编码RNA,参与肿瘤发生、发展和转移的多个过程。据报道,circRNA在外泌体中富集且稳定,它可能是一种有前途的癌症诊断生物标志物。
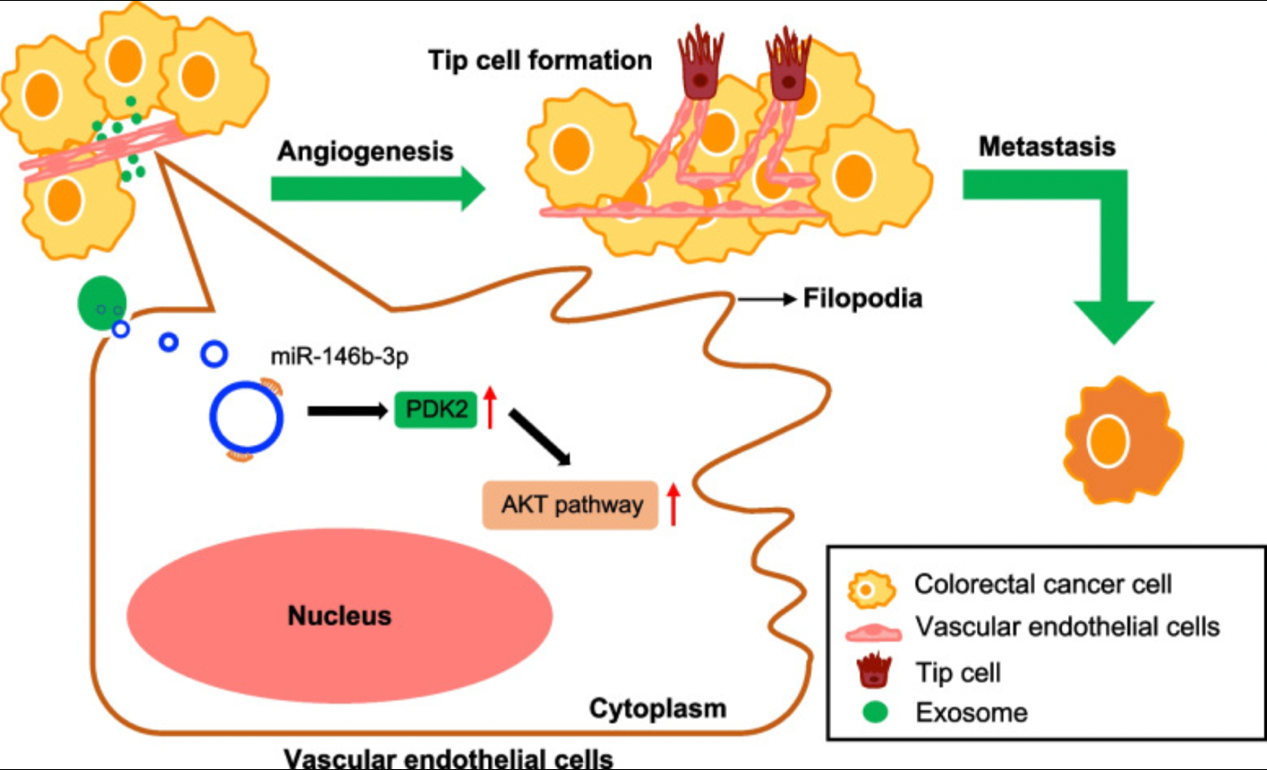
在本研究中,作者报道了结直肠癌细胞源性外体(CRC-CDEs)增强了内脏细胞迁移和管形成。新的发现表明,CRC CDEs诱导丝状体形成,导致内皮细胞倾斜。此外,作者还深入研究了转移或非转移CRC患者血清中circRNA的表达谱,发现了一种新的外泌体circRNA,circTUBGCP4,它促进了血管内皮细胞的功能障碍和肿瘤转移。机制上,作者发现circTUB-GCP4可以海绵miR-146b-3p激活Akt信号通路,同时证明外泌体circTUBGCP4的功能作用依赖于miR-146b-3p,miR-146b是抑制血管内皮细胞功能障碍的关键调节因子。这些发现可能为CRC转移提供一种新的抗血管生成治疗方法。
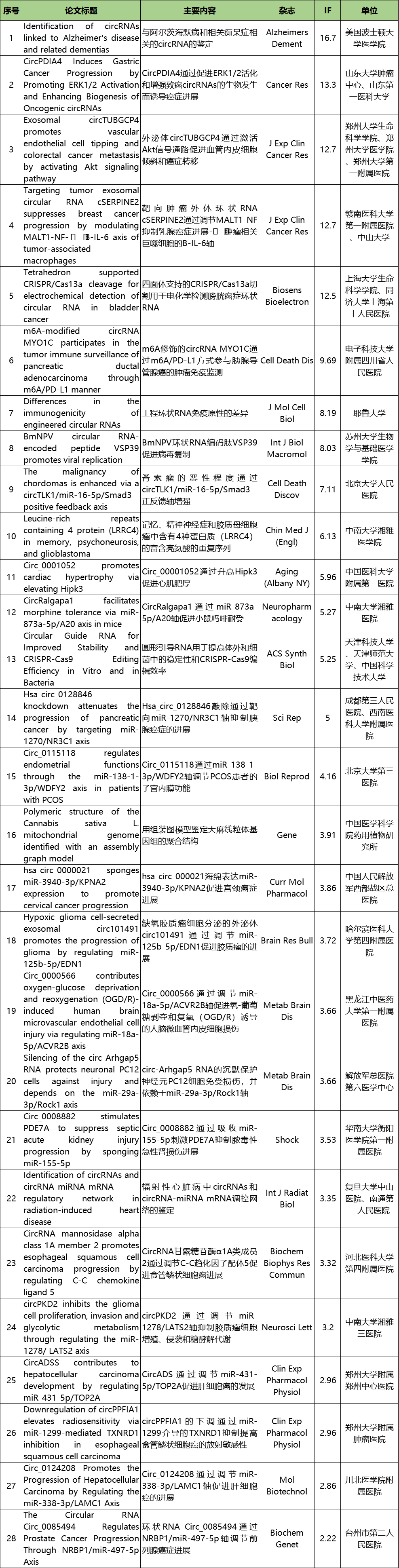
参考文献列表
转载请联系邮箱授权:circRNA@163.com
.png)