2020年6月27日,复旦大学附属中山医院的施国明、蔡加彬和柯爱武为共通讯作者在Molecular Cancer(IF=15.302)杂志上发表了一篇题为“Cancer cell-derived exosomal circUHRF1 induces natural killer cell exhaustion and may cause resistance to anti-PD1 therapy in hepatocellular carcinoma”的文章,阐述由肝癌细胞分泌的外泌体circUHRF1,可以通过miR-449c-5p/TIM-3途径,来抑制NK细胞功能、促进肝癌的免疫逃逸和提高抗PD1免疫疗法的耐药性,并为肝癌患者提供一种新的治疗策略,即靶向circUHRF1([1])。

自然杀伤(NK)细胞在先天性抗肿瘤免疫反应中起关键作用。最近,已经在包括肝细胞癌(HCC)在内的各种恶性肿瘤中证实了NK细胞功能障碍。然而,在人类肝癌中,NK细胞功能障碍的分子生物学机制仍不清楚。在本篇文章中,作者发现circUHRF1作为一种癌基因,在人肝癌组织中高表达,HCC患者血浆的circUHRF1主要由HCC细胞以外泌体的形式递送而来,它通过降解miR-449c-5p来上调其靶基因TIM-3的表达,从而抑制NK细胞功能、促进肝癌的免疫逃逸和驱动抗PD1免疫疗法的耐药性。因此,circUHRF1可能会成为HCC患者治疗的新靶点。
1、circUHRF1在肝癌组织中表达上调
在肝癌的发生发展中,UHRF1经常被上调,并在其病理过程中起关键作用。circRNA是由前体mRNA(pre-mRNA)反向剪接生成的单链闭合环状RNA,越来越多的研究表明,circRNA参与调控肝癌在内的多种癌症的发生发展,因此,作者想要探索UHRF1来源的circRNA是否也在肝癌的进展中起到重要作用。作者用qRT-PCR 技术检测UHRF1来源的14个circRNA在肝癌组织和配对癌旁组织中的表达水平。其中,hsa_cic_0048677(circUHRF1)是表达量最高的环状RNA,并在肝癌组织中上调。随后,作者检测了240例肝癌组织和配对癌旁组织中circUHRF1的表达差异,肝癌组织中circUHRF1的表达明显高于癌旁组织。接下来作者选取circUHRF1作为研究对象,探讨240例肝癌患者的circUHRF1表达与其临床病理特征之间的关系,与circUHRF1低表达患者相比,circUHRF1高表达患者的肿瘤体积较大,血液中NK细胞比例较低,微血管浸润较多。此外,还分析了肝癌患者的circUHRF1表达对临床预后的预测作用。Kaplan-Meier生存分析表明,circUHRF1高表达患者伴随临床预后不良。多因素分析表明,circUHRF1可以作为总生存期(OS)和术后复发的独立预测分子。综上所述,circUHRF1,在肝癌细胞中上调,并与患者的预后不良相关,它可能在肝癌的发生发展中起重要作用。
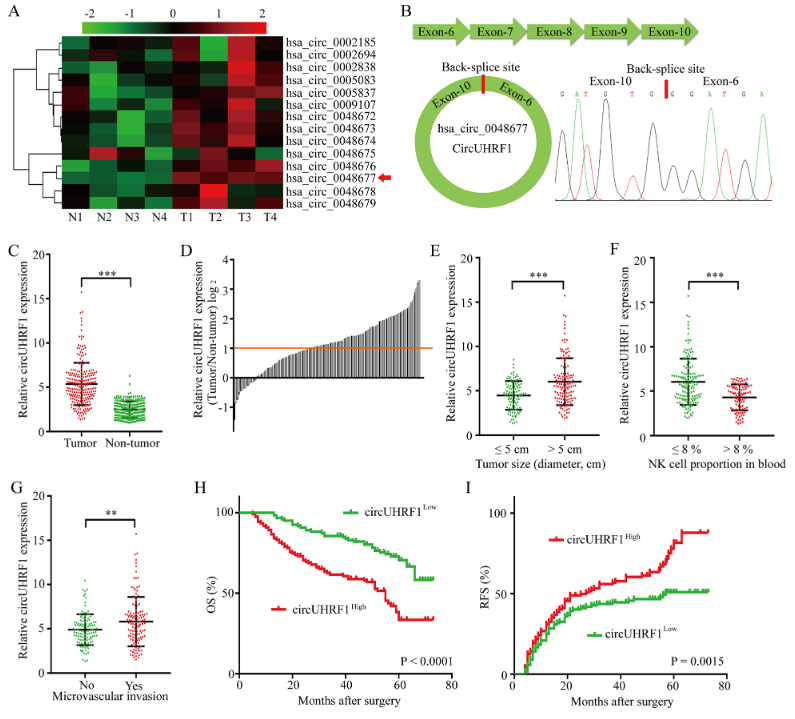
图1 circUHRF1在肝癌组织中表达上调
2、肝癌细胞可以通过外泌体将circUHRF1递送于肝癌患者血浆
以前有研究报道,circRNA可以通过外泌体在细胞间转运。因此,作者推测,circUHRF1可以通过外泌体由肝癌细胞转运至其他细胞内。为了验证这一假说,作者从六种肝癌细胞系上清液中分离出外泌体,随后使用透射电子显微镜(TEM)和western blotting对外泌体进行鉴定。然后,在六种HCC细胞系和相应的外泌体中进行qRT-PCR来分析circUHRF1表达,结果表明,相比于其他细胞系,HCCLM3和SMMC-7721细胞系中circUHRF1的表达最高。有趣的是,外泌体circUHRF1的表达与其亲代细胞内circUHRF1的表达水平相一致。
下一步,作者将探索circUHRF1是否可以由HCC细胞通过外泌体递送到HCC患者血浆中。随后,作者使用qRT-PCR检测健康供体、肝癌患者手术前、肝癌患者手术后和肝癌复发患者血浆中外泌体circUHRF1的表达水平。结果显示,与健康供体相比,HCC患者血浆外泌体circUHRF1的水平升高。此外,血浆外泌体circUHRF1的表达水平在肿瘤切除患者中降低,而在肿瘤复发患者中升高,这表明血浆外泌体circUHRF1主要来源于HCC细胞。有趣的是,在存在免疫逃逸机制的患者血浆中,外泌体circUHRF1水平的升高伴随着NK细胞比例降低,二者呈线性负相关。这些数据表明,外泌体circUHRF1可能是决定NK细胞相关免疫逃避的关键分子。
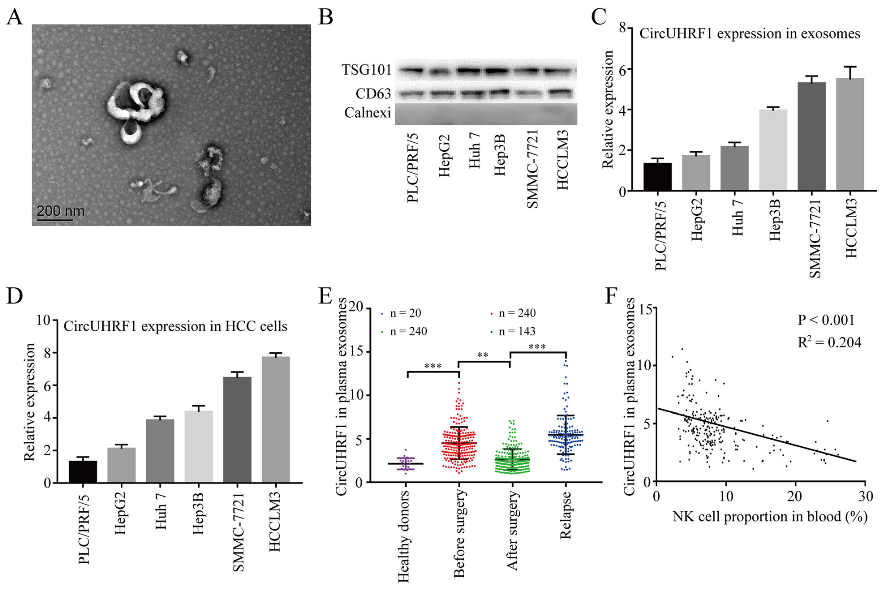
图2 肝癌患者血浆外泌体circUHRF1来源于肝癌细胞
3、肝癌细胞通过外泌体circUHRF1介导NK细胞功能障碍
为确定HCC细胞衍生的外泌体circUHRF1是否可以诱导NK细胞功能异常,作者将来自6位健康供体的NK细胞与HCCLM3和SMMC-7721细胞以1:1的比例共培养24小时,NK细胞随后再与K562细胞共孵育72小时。比较于单独培养的NK细胞,与SMMC-7721和HCCLM3细胞共培养的NK细胞在随后与K562细胞共孵育时,表现出IFN-γ和TNF-α分泌的显着受损,circUHRF1表达的显着增强,并且这两种作用可以被外泌体抑制剂GW4869所阻断。为了进一步验证HCC细胞是通过外泌体circUHRF1介导NK细胞功能障碍,作者构建shRNA慢病毒载体来敲低SMMC-7721和HCCLM3 细胞中的circUHRF1,这并不影响UHRF1 mRNA水平。结果表明,在敲低circUHRF1的肝癌细胞中,外泌体circUHRF1的表达显着降低,从而改善NK细胞中IFN-γ和TNF-α的分泌受损。这些结果共同表明,HCC细胞可以通过外泌体递送circUHRF1来损伤NK细胞功能。
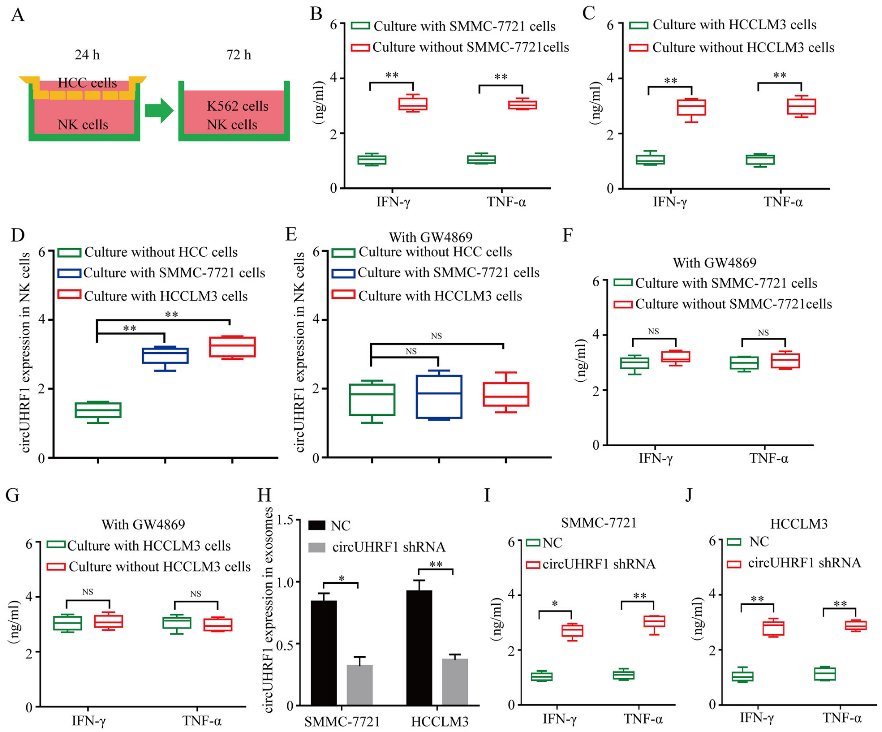
图3 外泌体circUHRF1可以抑制NK细胞功能
4、circUHRF1通过miR-449c-5p相关途径来抑制NK细胞功能
已有研究报道,circRNA主要作为miRNA海绵来发挥调控作用,它通过与miRNA结合来减少miRNA对下游靶基因的抑制作用,进而促进下游靶基因的表达。接下来,作者探索circUHRF1是否可以在人NK-92细胞中充当miRNA海绵分子来发挥作用。使用StarBase v3.0预测到可能与circUHRF1相结合的14个miRNA。为了验证这些候选miRNA与circUHRF1的直接作用,作者使用circUHRF1特异性探针在NK-92细胞中进行RIP实验,结果显示,比较于对照和其它miRNA,仅仅miR-449c-5p在circUHRF1上富集。因此,作者选取miR-449c-5p做进一步验证。在NK-92细胞中,进行抗AGO2抗体的RIP和生物素化miR-449c-5p的pull down实验,结果显示circUHRF1可以直接与miR-449c-5p结合,表明其具有miR-449c-5p海绵分子的潜力。最后,双萤光素酶报告基因实验证实,circUHRF1以序列依赖性的方式海绵吸附miR-449c-5p。令人惊讶的是,在NK-92细胞中,不仅过表达circUHRF1可以显著下调miR-449c-5p,而过表达miR-449c-5p同样可以显著抑制circUHRF1的表达。这些发现表明,在NK细胞中,circUHRF1和miR-449c-5P存在直接相互作用,它们是彼此的靶点。
因此,作者推测circUHRF1可能是通过下调miR-449c-5P,来抑制NK细胞功能。为了证实这一假设,作者在NK-92细胞中同时过表达circUHRF1和miR-449c-5P,来评估circUHRF1对miR-449c-5P的调控作用。结果显示,仅过表达miR-449c-5p的NK细胞表现出显著的抗肿瘤活性(促进NK细胞分泌IFN-γ和TNF-α),而同时过表达circUHRF1可以极大地削弱miR-449c-5p的抑癌作用,这表明HCC细胞衍生的外泌体circUHRF1是通过miR-449c-5p相关途径来抑制NK细胞功能。
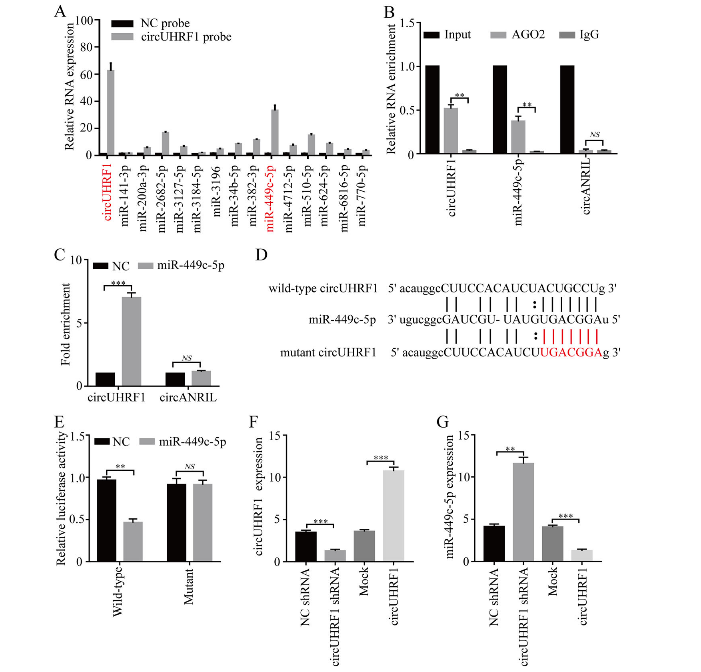
图4 circUHRF1通过miR-449c-5p相关途径来抑制NK细胞功能
5、circUHRF1通过miR-449c-5p来上调TIM-3的表达
已经证实,circUHRF1是通过调节miR-449c-5p相关通路来抑制NK细胞功能,接下来,作者的目的是寻找miR-449c-5p的下游靶基因。首先,作者使用StarBase v3.0来预测miR-449c-5p的下游靶基因,发现TIM-3的3’UTR存在miR-449c-5p结合位点。已知TIM-3是一种免疫调节受体,它参与抑制包括HCC在内的多种癌症的抗肿瘤免疫。因此,作者选取TIM-3做进一步分析,双萤光素酶报告基因实验证实,miR-449c-5p以序列依赖性方式直接结合于TIM-3的3’UTR。最后,为了阐述NK细胞中circUHRF1、miR-449c-5p和TIM-3三者之间的联系,作者在NK-92细胞中同时过表达miR-449c-5p和circUHRF1,使用qRT-PCR和western blot分别检测TIM-3的mRNA和蛋白水平。结果表明,仅过表达miR-449c-5p会显著下调TIM-3,而同时过表达circUHRF1会废除miR-449c-5p对TIM-3的抑制作用。这些实验表明,circUHRF1通过海绵吸附miR-449c-5p来上调TIM-3,进而导致NK细胞功能障碍。
为了进一步验证上述实验结果,即circUHRF1通过miR-449c-5p/TIM-3轴来抑制NK细胞功能。作者对源自40例HCC患者外周血的NK细胞,进行circUHRF1与miR-449c-5p/TIM-3表达的相关性研究。结果与预期相同,在外周血NK细胞中,circUHRF1与miR-449c-5p表达呈负相关,与TIM-3表达呈正相关。
先前有研究报道,在浸润肿瘤的NK细胞和CD8+ T细胞中,TIM-3的表达均上调。因此,作者想知道,HCC细胞衍生的外泌体circUHRF1是否也会抑制CD8+T细胞功能。遗憾的是,比较于单独培养的CD8+ T细胞,与SMMC-7721或HCCLM3细胞共培养的CD8+ T细胞在随后与K562细胞共培养时,并没有表现出明显的IFN-γ和TNF-α分泌受损,尽管circUHRF1的表达显着增加。作者还检测了miR-449c-5p在CD8+ T和NK细胞中的表达水平,发现miR-449c-5p的表达在NK细胞中显著高于CD8+ T细胞。这些结果表明circUHRF1 / miR-449c-5p / TIM-3轴对NK细胞的调节具有特异性,它在CD8+ T细胞中不起作用。
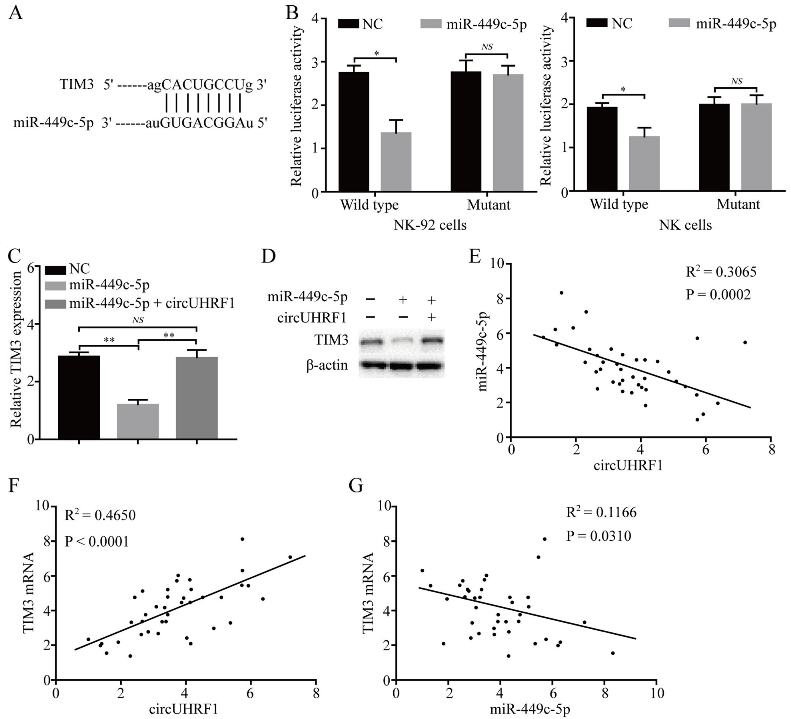
图5 circUHRF1通过miR-449c-5p/TIM-3途径来抑制NK细胞功能
6、circUHRF1以NK细胞依赖性方式促进HCC进展
为了进一步挖掘circUHRF1在肝癌中的作用,作者使用pLO5-ciR-circUHRF1慢病毒载体来上调PLC / PRF / 5细胞中circUHRF1的表达,过表达效率已被qRT-PCR证实。在过表达circUHRF1的HCC细胞中,外泌体circUHRF1水平也显著上调。接下来,作者使用PLC/PRF/5细胞构建肺转移的NOD/SCID小鼠模型(注射来自健康供者的NK细胞)。结果表明,在接种过表达circUHRF1细胞的肺转移小鼠内,血浆外泌体中circUHRF1水平更高,肺部的转移瘤结节更多及结节内NKG2D阳性细胞更少。这些结果表明,circUHRF1以外泌体和NK细胞依赖性的方式促进HCC进展。
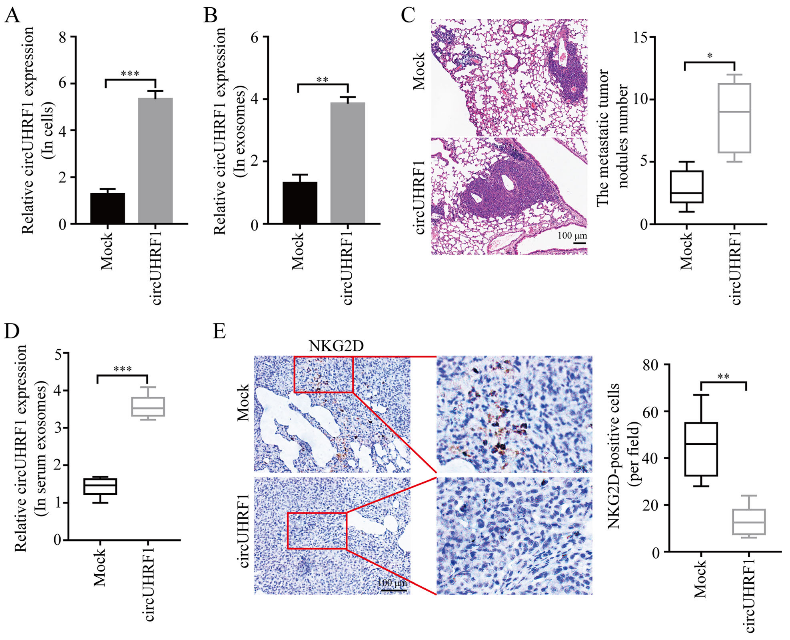
图6 circUHRF1以NK细胞依赖性方式诱导免疫逃避
7、circUHRF1可以提高肝癌对抗PD1治疗的耐药性
已经证实,过表达circUHRF1可以抑制HCC中NK细胞功能,作者接下来评估circUHRF1的过表达是否可以进一步阻止抗PD1治疗的抗肿瘤作用(Opdivo)。因此,作者回顾性分析了30例肝癌转移患者数据,这些肝癌患者在进行肝切除手术之前,接受过2-36个月的抗PD1治疗。在六个治疗周期后,使用CT评估疗效。经RECIST1.1分析,病情部分缓解(PR)的患者占3例,病情稳定(SD)的患者占7例,病情恶化(PD)的患者占20例。
然后,作者测量circUHRF1的表达水平,结果表明,PD组的circUHRF1水平明显高于SD组和PR组。为了进一步探讨circUHRF1与免疫逃避之间的关系,作者检测了30例HCC患者组织中NKG2D的表达水平。结果表明,与抗PD1治疗敏感的HCC患者相比,抗PD1治疗耐药的HCC患者中NKG2D的阳性细胞数明显减少。散点图分析显示,HCC组织中circUHRF1表达与NKG2D的阳性细胞数呈负相关。为了直接评估circUHRF1对抗PD1治疗的影响,作者通过皮下植入circUHRF1基因敲低的HCCLM3细胞或相应的阴性对照细胞来构建小鼠移植瘤模型。结果表明,植入circUHRF1基因敲低细胞的小鼠对抗PD1治疗敏感,并伴随总生存率的提高。综上所述,过表达circUHRF1可以提高HCC对抗PD1治疗的耐药性,而靶向circUHRF1可能是恢复HCC对PD1治疗敏感性的有效方法。
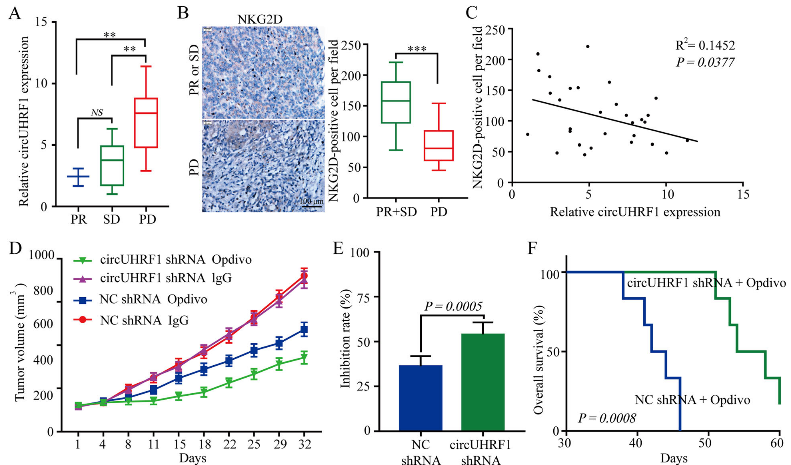
图7 高表达的circUHRF1与HCC患者抗PD1治疗的耐药性相关
参考文献:[1] Zhang PF, Gao C, Huang XY, et al. Cancer cell-derived exosomal circUHRF1 induces natural killer cell exhaustion and may cause resistance to anti-PD1 therapy in hepatocellular carcinoma. Mol Cancer. 2020;19(1):110. Published 2020 Jun 27. doi:10.1186/s12943-020-01222-5
.png)