2020年2月10日,南方医科大学顺德医院的黄裕立教授在Theranostics (IF= 8.063)杂志上发表了一篇题为“环状RNA-蛋白质互作:功能,机制和验证方式”的综述文章,该文章回顾了目前circRNA-蛋白质互作领域已知的内容,介绍了研究这种互作的常规方法,并提出了对于这类互作的一些新颖的看法。([1])

CircRNA是一类内源性共价闭合的环状RNA,不存在5’帽子和3’尾巴。目前发现人脑中有20%的基因可以转录产生circRNA,而心脏中这个比例只有9%。而且在低增殖活性的细胞(如心肌细胞)要比高增殖活性细胞(如肝细胞)表达量要更高,并且表现出随年龄增长的累积效应。由于circRNA的结构特点,使其在细胞内比线性RNA更不易受到核酸酶的降解,而且表达方式呈现出组织、细胞、发育阶段的特异性,因此被认为可以用作潜在的疾病分子标志物。
目前认为,circRNA除了作为miRNA分子海绵(miRNA sponges)外,在生物体内扮演的功能包括:蛋白质分子海绵(protein sponges),蛋白诱捕陷阱(decoys),蛋白质支架(scaffolds),蛋白质招募(recruiters),甚至翻译产生蛋白质。
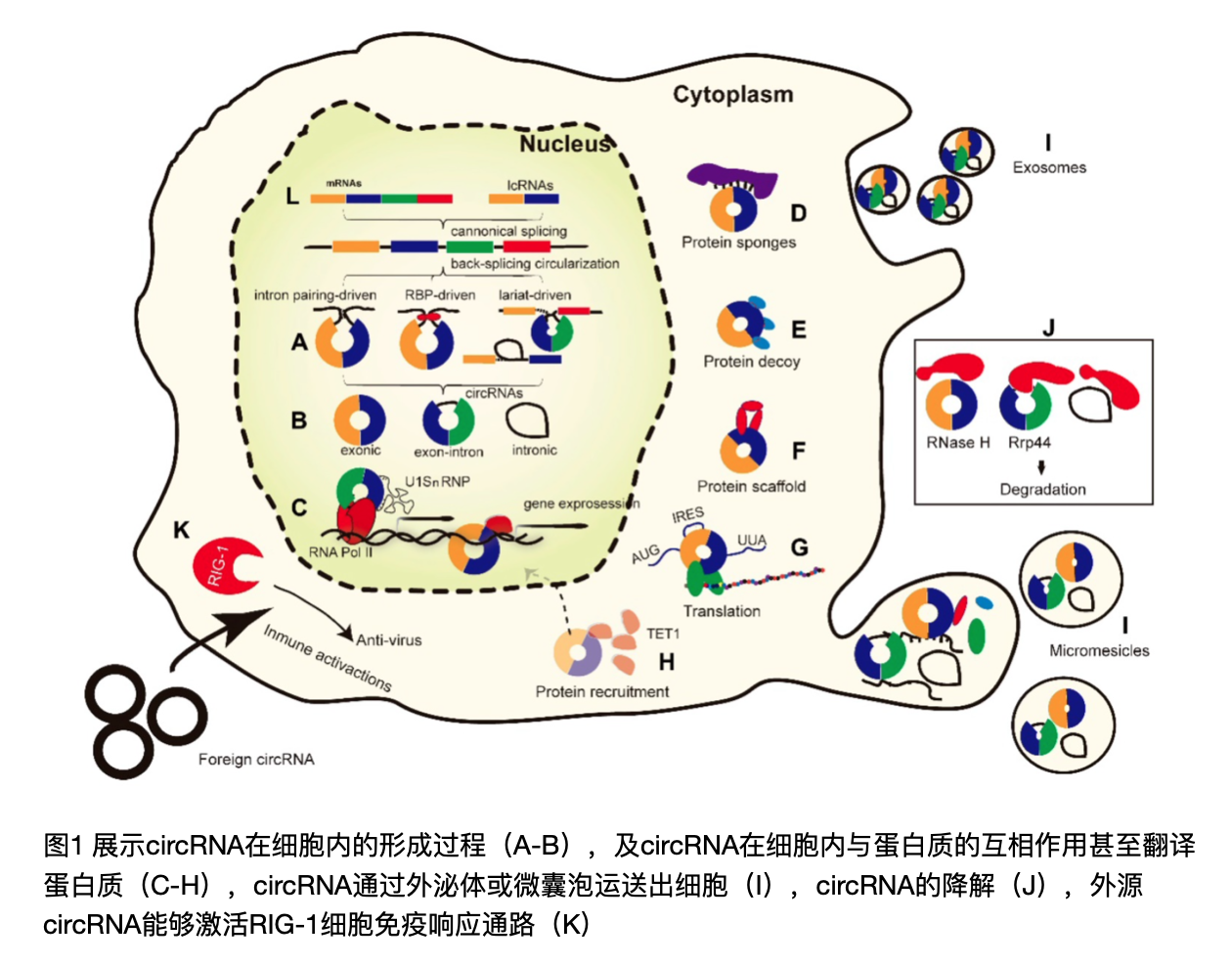
这类功能都涉及到circRNA和蛋白质的相互作用,已经有研究表明除了常规的识别特定序列的结合方式外,circRNA形成的特定三维结构也会影响到与蛋白质之间的相互作用。而这类特定的三维结构往往会受到细胞内离子类型、浓度的影响导致circRNA表达模式呈现组织、细胞、发育阶段特异性的现象。
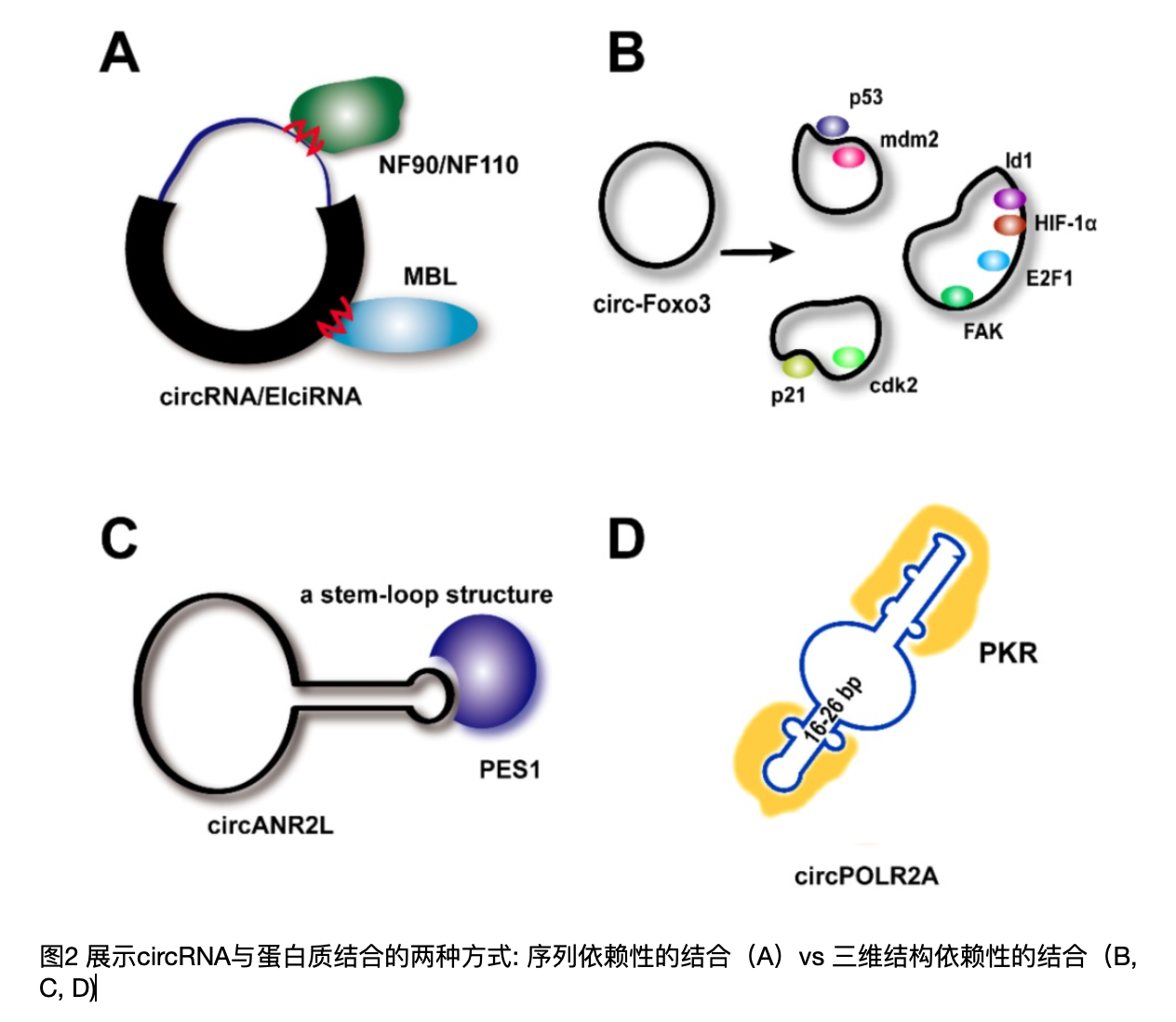
CircRNA和蛋白质的相互作用对于circRNA的合成与降解,和蛋白的表达与功能都会产生影响。在与circRNA结合的蛋白质中最著名的就是RNA结合蛋白(RNA binding proteins)。已经有研究表明circRNA的生物合成过程受到RBPs、转录因子、顺式调控元件和反式剪切因子的混合作用调控。
目前用来做circRNA-蛋白质相互作用研究的方法有:RNase酶保护实验,RNA pull-down,抗体依赖的RIP,电泳迁移分析法(EMSA),荧光原位杂交法(FISH)。
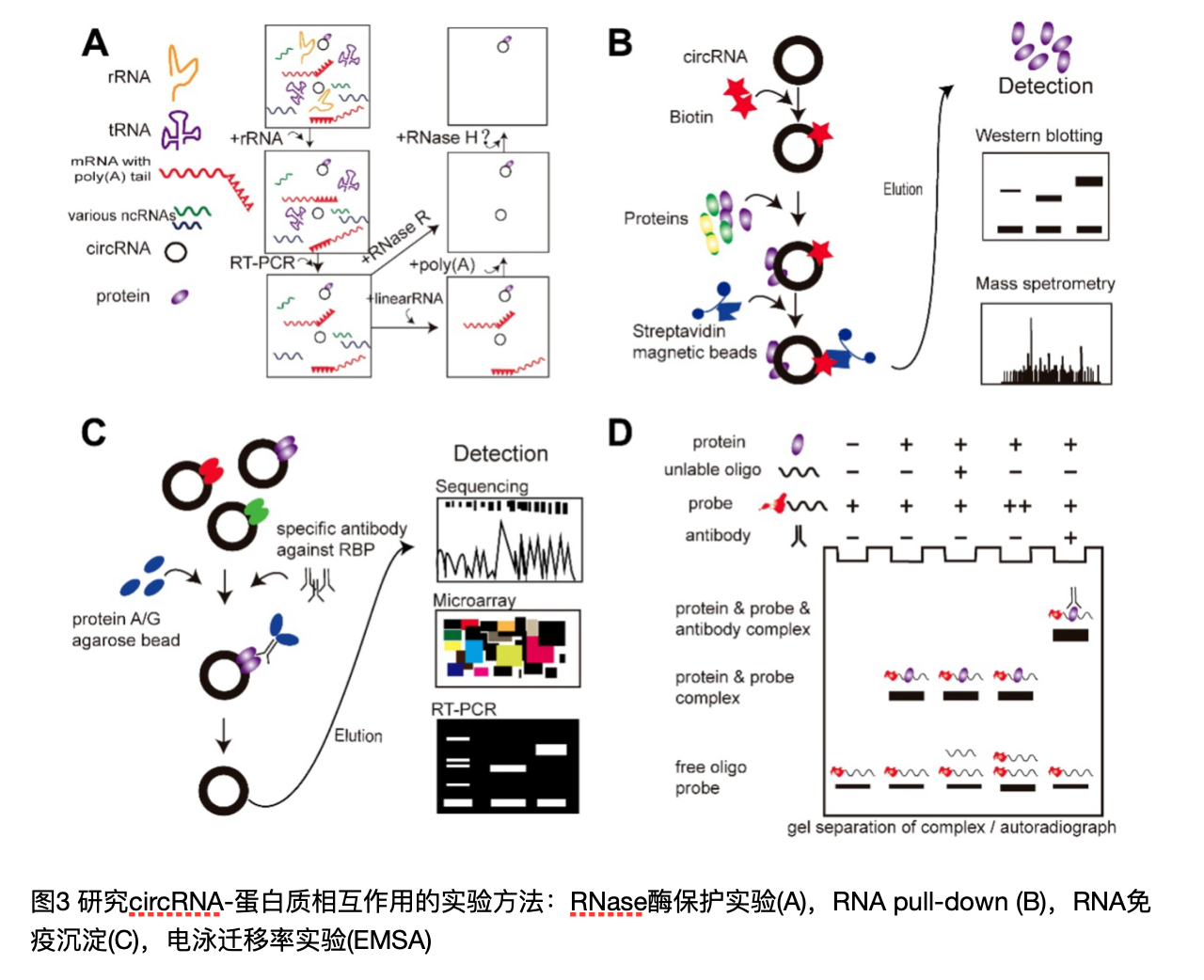
受限于技术上的限制,虽然已经证明circRNA在体内发挥了重要的作用,而且参与与蛋白质结合的circRNA的数量也很多,但是能够直接揭示circRNA和蛋白质互作的机制的技术依然很有限。而且缺乏有效的方法复原circRNA在体内的三维结构,也成为研究依赖三位构象与蛋白质结合的那一类circRNA的障碍。并且目前研究circRNA方面有一个重要的领域是外泌体中的circRNA,外泌体中的circRNA除了作为细胞间信号传导的重要方式,也是有效降低细胞体内circRNA含量的重要方式,但是外泌体形成过程中是如何富集circRNA的作用机制也还是不清楚。另一个有趣的领域是细胞免疫。早在2017年,Stanford University School of Medicine的Howard Y. Chang就证明细胞能够识别细胞内源产生的circRNA和外源的circRNA,并激活对于病毒感染的自体免疫反应。然而到了2019年,Anderson et al. 却报道内源的circRNA没能激活免疫通路,之前之所以产生那样的结果是因为样本的纯化不充分,样本中混了含有5’磷酸基团的线形RNA。随后Chang的团队反驳了这种说法,他们证实是人体circRNA受到m6A的修饰阻止了免疫基因的活化。没有受到修饰的circRNA可以直接激活RNA识别受体(RIG-1),并且外源的circRNA也可以通过这种方法激活机体的免疫反应。
目前在circRNA的研究领域还有很多的困难和争论,希望能够在今后有更多人进入circRNA的研究中,因为circRNA将很有可能作为新一代的疾病分子标志物和治疗靶点在临床上发挥作用。
参考文献
- Huang A, Zheng H, Wu Z, Chen M, Huang Y. Circular RNA-protein interactions: functions, mechanisms, and identification. Theranostics 2020; 10(8):3503-3517. doi:10.7150/thno.42174.
.png)